La médecine translationnelle est une composante majeure de la recherche et du développement clinique. Il s’agit d’une discipline transversale entre chercheurs, cliniciens et patients dont l’enjeu est de permettre de transférer une innovation du stade de la recherche à celui du développement clinique chez l’homme et nourrir la recherche fondamentale avec des observations issues de la recherche clinique.
Eclairages avec Fabien Schmidlin, directeur du département médecine translationnelle chez Servier.
La médecine translationnelle se situe entre la recherche fondamentale, dont le travail consiste à comprendre les mécanismes du développement d’une maladie, et la recherche clinique qui vise à évaluer l’efficacité et la tolérance de nouveaux traitements sur les patients.
Cette discipline collaborative joue un rôle essentiel dans la traduction des découvertes scientifiques en nouveaux traitements pour améliorer la santé des patients. La médecine translationnelle allie les compétences des chercheurs, pharmacologues, et des cliniciens pour évaluer de nouveaux traitements et in fine accélérer toutes les étapes du développement d’un médicament. Elle s’applique à toutes les pathologies.
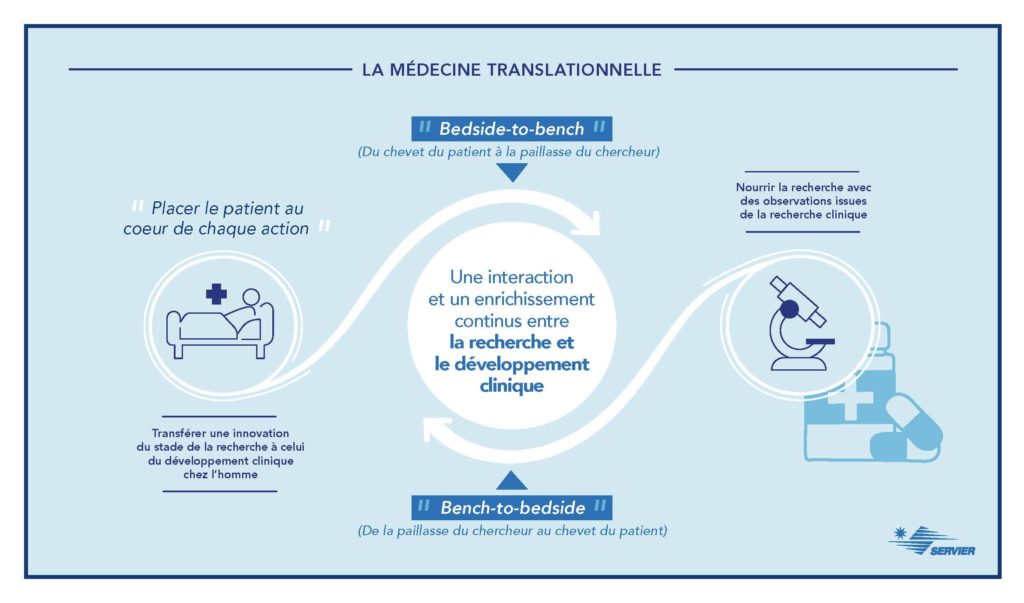
En partant des observations cliniques et du besoin médical des patients, « Bedside to Bench », la Médecine Translationnelle supporte la recherche de nouvelles molécules en accélérant leur évaluation chez les patients, « Bench to Bedside ».
Des objectifs au bénéfice des patients
Pour Fabien Schmidlin, « Auparavant, il existait un décalage important entre le monde de la recherche en laboratoire et celui du développement clinique du médicament. Aujourd’hui, la médecine translationnelle fait ce lien plus direct entre recherche et soins ; ce qui, in fine, accélère les prises de décisions pour la mise sur le marché d’une molécule ».
« Avant, avec une même molécule, on essayait de traiter tous les types de cancers » souligne Fabien Schmidlin. « Aujourd’hui, on essaye très tôt d’identifier des sous-populations de patients qui vont répondre efficacement au traitement. C’est ce qu’on appelle la médecine personnalisée. Aujourd’hui on a des thérapies ciblées pour certains cancers où l’on observe un taux de réponse jusqu’à 90 % ».
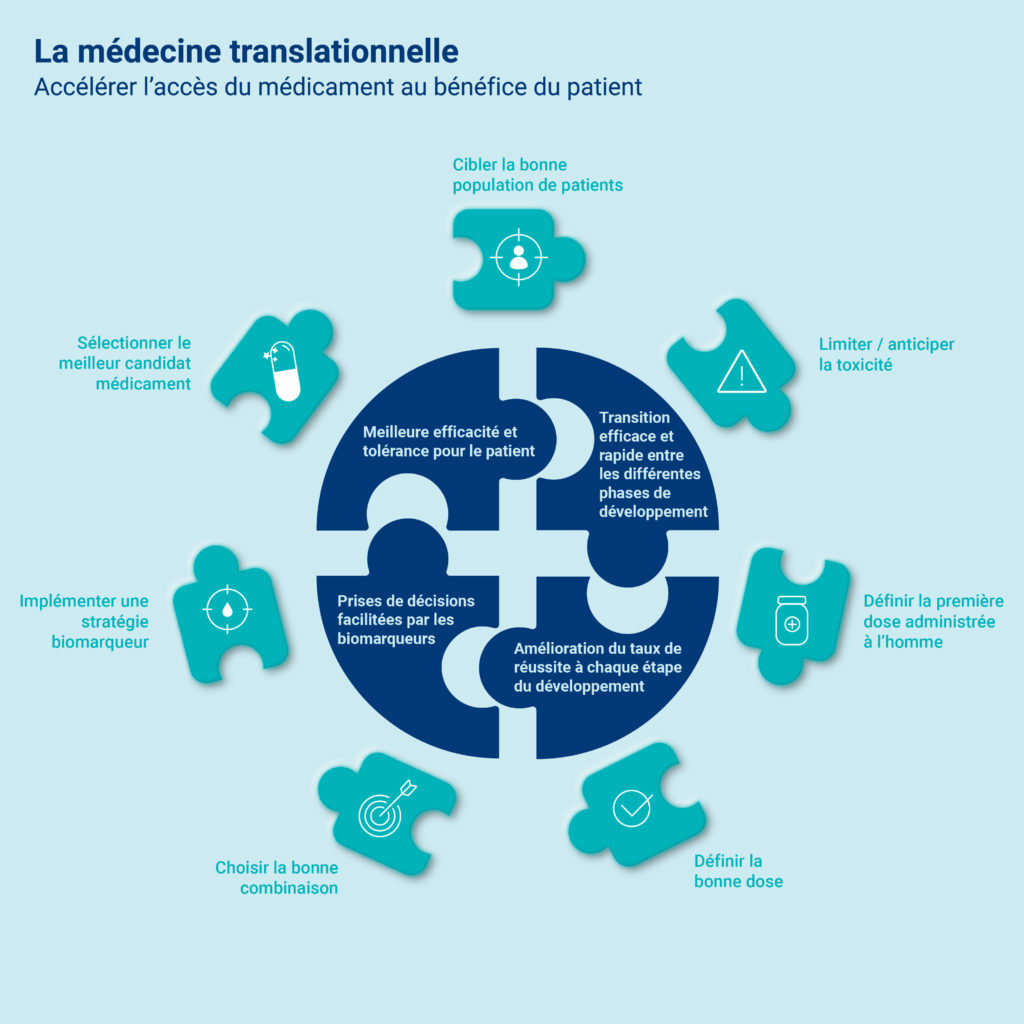
La médecine translationnelle chez Servier
En 2020, Servier a créé un département dédié à la médecine translationnelle.
Il a pour objectif de contribuer, en support à la recherche, à une transition efficace et rapide du portfolio de molécules du Groupe entre la phase préclinique (qui permet d’évaluer une molécule sur des cellules en culture in vitro et chez l’animal in vivo) et la FIM (« first in man » : 1ère dose administrée à l’homme), qui est la première étape des essais cliniques.
Ce département en interaction étroite avec les autres acteurs de la R&D doit permettre d’accélérer le développement de nouveaux médicaments jusqu’à leur autorisation de mise sur le marché au bénéfice des patients.
« Le patient est au cœur de la démarche et il joue un rôle fondamental dans ce processus de découverte de nouveaux traitements » précise Fabien Schmidlin. « Son engagement permet de collecter des données cliniques et des échantillons biologiques qui seront essentiels pour la mise à disposition de nouvelles solutions thérapeutiques. »
Au cœur de la médecine translationnelle : les biomarqueurs
Quel rôle dans le développement d’un médicament ?
Les biomarqueurs sont essentiels dans l’ensemble du processus de développement du médicament. Ils facilitent de plus en plus les prises de décisions à chaque étape. Ces biomarqueurs permettent de suivre ou de prédire l’efficacité et la sécurité du produit pendant le développement ou de sélectionner les patients répondeurs.
Dans les programmes de médecine translationnelle, le développement des biomarqueurs est crucial. Il en existe de différents types qui remplissent plusieurs objectifs :

ET SERVIER ?
Servier s’engage dans une stratégie innovante, et sécurisante pour les patients, pour mener essentiellement des études cliniques comprenant des biomarqueurs. Cette stratégie « biomarkers driven » doit renforcer le développement de thérapies ciblées au bénéfice du patient.
Aujourd’hui, une grande majorité des biomarqueurs en cours de développement au sein de Servier sont dédiés à l’oncologie. Cependant, la recherche de nouveaux biomarqueurs offre de nouvelles perspectives dans le développement de molécules pour les maladies auto-immunes (le lupus par exemple) ou les maladies neurologiques.
Le département du développement de biomarqueurs Servier, créé récemment, se veut être un véritable accélérateur de la médecine personnalisée, pour améliorer la prise en charge thérapeutique et la qualité de vie du patient.
